應用教學
應用教學
代謝型麩胺酸受體 (mGluR) 簡介
![]() APR 29 ,2022
APR 29 ,2022
總論
代謝型麩胺酸受體 (Metabotropic glutamate receptors, mGluRs) 是一種 G蛋白偶連受體 (G-protein coupled receptors, GPCRs),其作用為將麩胺酸固定並進行訊息傳遞 [1,2,3]。 mGluRs 也有調節其他受器的功能,像是調節 NMDA、 AMPA 與 K他命受器等等,這些受器皆與不同種類的神經功能與疾病息息相關, 例如急性/慢性疼痛、學習記憶相關功能、焦慮、精神疾病、癲癇、藥物成癮、神經退化性疾病與腦損傷等 [4,5,6,7,8,9,10]。 這篇文章將會為mGluR作個簡單的介紹。
代謝型麩胺酸受體種類與分類
目前我們可以將已知且可在中樞/週邊神經系統的mGluR分為以下數個組別: Group I (mGlu1 and mGlu5)、Group II (mGlu2 and mGlu3) 以及 Group III (mGlu4, mGlu6, mGlu7 and mGlu8) [11]。 分為此三個組別其依據為結構相似度、藥理性質以及胞內訊息傳遞機制 [12]。
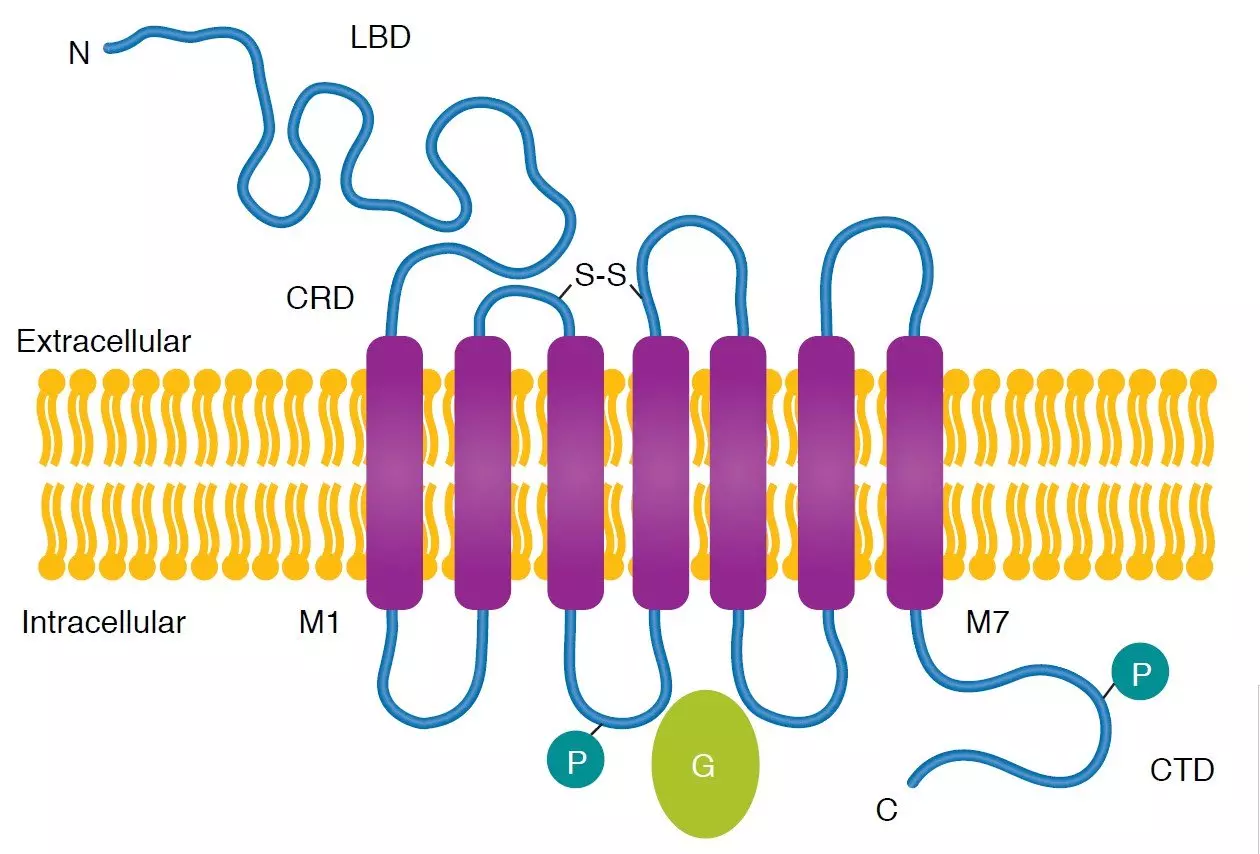 mGluR 的結構
mGluR 的結構
mGluR 與 GABAB 受體、 Ca2+感應受體、費洛蒙受體以及味覺受體結合成一個與腎上腺素型GPCR大相逕庭的蛋白質群集 (Superfamily)。兩個受體群集都具有 7 個跨膜結構域基序 (TMD),但與腎上腺素型 GPCR 相比,mGluR具有更大的 N 端結構域並且沒有大的螺旋間環 ,此外, mGlu1、mGlu3、mGlu5、mGlu6、mGlu7 以及 mGlu8 受體皆有發現選擇性剪接的版本
mGluR 二聚化 (dimerization)
mGluRs 可以被單獨活化,也可以作為二聚體 (dimer) 存在。 這涉及在兩個單獨受體的 N 端結構域之間形成二硫鍵, 在非還原條件下,幾乎所有 mGluR 都以二聚體這種形式存在 [13]。因此,單個受體蛋白可被視為一個次單位 (Subunit),二聚體才是一個完整的受體。
配體結合區 (Ligand Binding Domain, LBD) - 捕蠅草結構
mGluR的大型 N 端結構包含配體結合位點,該位點由兩個鉸接的球狀結構 - “捕蠅草結構”(VFD) 形成。 麩氨酸的結合使得捕蠅草結構的兩個端點結構關閉,使得 TMD 發生變化,進而導致 G 蛋白的活化[14]。
mGluR的活化與G蛋白的堆疊
麩胺酸是中樞神經系統(Central Nervous System, CNS)的主要的興奮性胺基酸神經傳導物質,可用來活化mGluR。這會導致相關 G 蛋白的活化,造成結合的 GTP 被交換為 GDP,促使第二信使 (Second Messenger) 被活化,導致去極化和興奮性神經訊號傳遞 [15]。
若今天被活化的mGluR不同,接下來被活化的第二信使可能也會有所差異。 Group I mGluRs 會通過Gq蛋白與磷脂酶C (Phospholipase C, PLC) 成對結合並活化,這個活化會導致細胞內存的鈣離子被釋出且活化蛋白激酶C (Protein Kinase C, PKC),並造成IP3與二酸甘油脂(Diacylglycerol)的濃度增加[16]。Group II and III mGluRs 主要會與 Gi/o型G蛋白作用並抑制腺苷酸環化酶(adenylyl cyclase)[15]。這些G蛋白會與離子通道蛋白或是PLC成對結合,且同時擁有活化腺苷酸環化酶並抑制cAMP合成的功能。
mGluR 的功能
mGluRs 參與了許多種類的生物作用,包含了以下反應:
- 慢速的興奮性或抑制性突觸反應
- 鈣與鉀離子以及非選擇性陽離子通道的調節
- 神經傳導物質釋出之調控
- 長期增強/抑制現象 (LTP/LTD) 之生成
- 不同種類的記憶生成
- 配體門麩胺酸受器(Inootropic glutamate receptor, iGluR) 運輸(trafficking)之調節
- 調控NMDA受器調節之突觸訊息傳遞
- 調控神經發育
- 神經元與膠細胞之間的訊息傳遞
代謝型麩胺酸受體與突觸可塑性和學習記憶密切相關,且其作用機制非常複雜。 由活體動物實驗所得到的研究結果指出了,mGlu 受體參與海馬迴依賴性學習取決於要學習的事物及其與突觸可塑性的關係。 在電生理的研究則指出了 mGlu 受體在海馬迴依賴性突觸可塑性的持續起著至關重要的作用。
長期增強現象(LTP) 和長期抑制現象(LTD)代表了神經可塑性的最佳表徵形式。 長期增強現象是某些類型的突觸刺激(例如長時間的高頻率刺激)導致突觸傳遞強度長期(至少數小時)增加的生理現象。 LTD則是相反,為接受刺激後突觸傳遞的功效和強度的長期下降的現象 [17]。
近年來的研究指出Group II 與Group III的mGluR在長期增強現象的調節中所扮演的角色可能沒有我們之前想得那麼重要,但在維持長期抑制現象以及長期的空間記憶生成中則是至關重要。相較之下,Group I的mGluR則是在LTP/LTD的生成以及海馬迴介入的記憶生成皆非常重要 [18]。
以下表格總結了不同組別的mGluR會對LTP與LTD的生成調控有何影響, mGluR與LTD之間涉及了多種的訊號傳遞機制,我們也由此可見神經可塑性是多麼複雜的一門學問。針對影響最甚的mGlu1與mGlu5,您也可以參考我們精心整理的海報 點我下載
表格1:mGluR對於長期增強現象的影響
| mGluR group | Group I | Group II | Group III | |
| mGluR subtype | mGlu1 | mGlu5 | mGlu2, mGlu3 | mGlu4, mGlu7, mGlu8 |
| Agonists | - | facilitate STP into persistent LTP | raise LTP threshold | raise LTP threshold |
| Antagonists | impair CA1 & DG persistent LTP by reducing induction | reduce induction & prevent maintenance in CA1 & DG | No effect | No effect |
| Knockout | impaired CA1 LTP, impaired mf LTP | impaired CA1 & DG LTP, normal mf LTP | normal mf LTP | - |
表格2:mGluR對於長期抑制現象的影響
| mGluR group | Group I | Group II | Group III | |
| mGluR subtype | mGlu1 | mGlu5 | mGlu2, mGlu3 | mGlu4, mGlu7, mGlu8 |
| Agonists | - | facilitate STD into persistent LTD | facilitate STD into LTD | facilitate STD into LTD |
| Antagonists | impair LTD by reducing induction and preventing maintenance in CA1 & DG | impair LTD in CA1 & DG | block persistent LTD | block persistent LTD |
| Knockout | normal CA1 LTD | - | - | - |
縮寫說明:dentate gyrus (DG); long-term potentiation (LTP); long-term depression (LTD); mossy fibre (mf); short-term depression (STD); short-term potentiation (STP)
變塑性(Metaplasticity)也由 mGluRs 介導,其中突觸的前期變化和 mGluRs 的前期活化會改變突觸可塑性的表現。 透過影響突觸處的蛋白質合成使得蛋白質量增加,Group I mGluR 可讓 LTP更持久與穩定。 第二組 mGluR 引發增加齒狀回 (Dantate Gyrus, DG) LTD 生成並抑制 LTP 的產生。[18]
目前我們認為mGluR對突觸可塑性產生影響的機制包括了下列數項:
- 產生訊號堆疊(signaling cascade)藉此使得突觸可塑性更加穩定
- 調節與神經可塑性息息相關的NMDA受體[19]
- 影響蛋白質之間形成鷹架(scaffold)結構,進而抑制突觸間的訊號傳遞[20]
病理學特徵
對於學習記憶來說,代謝型麩胺酸受體(metabotropic glutamate receptors)是至關重要的,目前已知有數種學習記憶功能缺失的疾病與mGluR功能異常有關,例如X染色體脆折症、智能障礙以及自閉症[21,22]。針對mGluR功能缺失的治療一直都是一個有且潛力且熱門的研究項目,其研究結果也已被用在許多神經相關疾病上[8,9,10]。
藥理學特徵
mGluR會被以下數種內生性的配體活化: L-glutamic acid、L-serine-O-phosphate、N-acetylaspartylglutamate (NAAG) 以及 L-cysteine sulphinic acid. 在最近這幾年,越來越多針對不同組別與亞型(subtype)mGluR擁有選擇性的配體被發現。
組別選擇性(Group selectivity)
選擇性的mGLuR促進劑的例子包含了以下: (1S,3R)-ACPD 以及 L-CCG-I,它們只針對Group II的mGluR進行有限度的活化。至於mGluRu抑制劑的例子有LY 341495,這種抑制劑可以阻斷mGlu2 與 mGlu3 的生成使其維持在極低濃度、 mGlu8 亦被抑制但濃度略高,至於 mGlu4、mGlu5與mGlu7 影響則不會那麼大 (但還是有些微抑制)。
Group-I mGluR 可以被 (S)-3,5-DHPG 所活化。Group-II mGluR 則是可以被LY 354740活化,且同時可被(+/-) -LY395756所抑制。Group-III mGluR 則是可以被 L-AP4 與(R,S)-4-PPG所活化,其抑制劑為MSOP。
亞型選擇性(Subtype selectivity) 促進/抑制劑
目前已經有許多種類的亞型促進/抑制劑被發現且問世,例如CHPG (mGlu5 促進劑), MTEP (mGlu5 抑制劑), AMN082 (mGlu8 促進劑) MDCPG (mGlu8 抑制劑) and XAP 044 (mGlu7 抑制劑)
調節因子(Modulators)
除了一般可直接與麩胺酸上辨識區連接的的正構(orthosteric)配體之外,亦有形態不同的異構(allosteric)調節因子被發現。正極異構調節因子(Positive allosteric modulators, PAMs)通常在沒有促進劑協助或是受體未被顯著活化的正構配體與胺基酸的反應中作為一個增效劑(potentiator), 例如 BINA (對應mGlu2的PAM)、VU0361737 (對應mGlu4) 以及 VU 0360172 (對應mGlu5)。負極異構調節因子(Negative allosteric modulators, NAMs) 包含了ADX 10059 (對應mGlu5) 以及 ML 289 (對應mGlu3).
New tools for modulating mGluR desensitization
除了上述的亞型選擇性促進/抑制劑以及調節因子之外,近期亦有亦有一些可用於GPCR脫敏(desensitization)相關研究藥物被研發出來,例如 GRK2/3 抑制劑 Cmpd 101。
有關代謝型麩胺酸受器受體之配體之總覽,您可以見下方表格或是 點選此連結
Group I (mGlu1, mGlu5) receptors
| (S)-3-Hydroxyphenylglycine | mGlu1 促進劑 |
| (R,S)-3,5-DHPG | 選擇性 mGlu1/mGlu5 促進劑 |
| (S)-3,5-DHPG | 選擇性 mGlu1/mGlu5 促進劑 |
| L-cysteinesulfinic acid monohydrate | mGlu1α / mGlu5a 促進劑 |
| CHPG | 選擇性 mGlu5 促進劑 |
| (S)-4-Carboxyphenylglycine | 競爭性選擇性 group 1 mGlu 抑制劑 |
| JNJ 16259685 | 強效選擇性非競爭性 mGlu1 抑制劑 |
| MPEP hydrochloride | 強效選擇性 mGlu5 抑制劑 / mGlu4 正極異構調節因子 |
| MTEP hydrochloride | 選擇性非競爭性 mGlu5 負極異構調節因子 |
| VU 0360172 hydrochloride | 強效選擇性非競爭性 mGlu1 抑制劑 |
Group II (mGlu2, mGlu3) receptors
| LY 354740 hydrate | 強效選擇性 group II receptor 促進劑 |
| LY 341495 | 強效選擇性 group II mGlu 受體抑制劑 |
| MAP4 | 競爭性選擇性 mGlu3 抑制劑 |
| LY 487379 | 選擇性 mGlu2 正極異構調節因子 |
| BINA | 強效選擇性 mGlu2 正極異構調節因子 |
| ML 289 | 選擇性 mGlu3 負極異構調節因子 |
Group I & II receptors
| ±-trans-ACPD | 選擇性 group I 與 group II mGlu 促進劑 |
Group III (mGlu4, mGlu6, mGlu7, mGlu8) receptors
| AMN 082 dihydrochloride | 強效選擇性 mGlu7 促進劑 |
| (S)-3,4-DCPG | 強效選擇性 mGlu8a 促進劑 |
| L-AP4 | 強效選擇性 mGlu group III 促進劑 |
| Cinnabarinic acid | 選擇性 mGlu4 促進劑 |
| XAP 044 | 新穎選擇性 mGlu7 抑制劑 |
| MDCPG | 選擇性 mGlu8 受體抑制劑 |
| MSOP | 選擇性 group III mGlu 抑制劑 |
| VU0155041 sodium salt | 水溶性mGlu4 正極異構調節因子 |
| AZ 12216052 | 新穎 mGlu8 正極異構調節因子 |
mGlu General
| L-Quisqualic acid | mGlu / AMPA 受體促進劑 |
參考文獻
1. Sladeczek F et al (1985) Glutamate stimulates inositol phosphate formation in striatal neurones.Nature. 317(6039):717-9. http://www.ncbi.nlm.nih.gov/pubmed/2865680
2. Nicoletti et al (1986) Coupling of inositol phospholipid metabolism with excitatory amino acid recognition sites in rat hippocampus.J Neurochem. 46(1):40-6 http://www.ncbi.nlm.nih.gov/pubmed/2866236
3. De Blasi et al (2001) Molecular determinants of metabotropic glutamate receptor signaling. Trends Pharmacol Sci. 22(3):114-20 http://www.ncbi.nlm.nih.gov/pubmed/11239574
4. Lees et al (2013) Peripheral group II and III metabotropic glutamate receptors in the knee joint attenuate carrageenan-induced nociceptive behavior in rats.Neurosci Lett. 10;542:21-5 http://www.ncbi.nlm.nih.gov/pubmed/23500028
5. Mukherjee S et al (2013) Role of metabotropic glutamate receptors in persistent forms of hippocampal plasticity and learning. Neuropharmacology. 66:65-81. http://www.ncbi.nlm.nih.gov/pubmed/22743159
6. De Filippis et al (2015) The role of group II metabotropic glutamate receptors in cognition and anxiety: comparative studies in GRM2(-/-), GRM3(-/-) and GRM2/3(-/-) knockout mice.Neuropharmacology. 89:19-32 http://www.ncbi.nlm.nih.gov/pubmed/25158312
7. Walker and Conn (2015) Group I and group II metabotropic glutamate receptor allosteric modulators as novel potential antipsychotics.Curr Opin Pharmacol. 20:40-5. http://www.ncbi.nlm.nih.gov/pubmed/25462291
8. Mercier MS, Lodge D (2014). Group III metabotropic glutamate receptors: pharmacology, physiology and therapeutic potential. Neurochem Res. 39(10):1876-94 http://www.ncbi.nlm.nih.gov/pubmed/25146900
9. Yin S, Niswender CM (2014) Progress toward advanced understanding of metabotropic glutamate receptors: structure, signaling and therapeutic indications. Cell Signal. 26(10):2284-97 http://www.ncbi.nlm.nih.gov/pubmed/24793301
10. Nicoletti F, Bruno V, Ngomba RT, Gradini R, Battaglia G. Metabotropic glutamate receptors as drug targets: what's new? Curr Opin Pharmacol. ;20:89-94 http://www.ncbi.nlm.nih.gov/pubmed/25506748
11. Foord SM et al (2005) Pharmacol Rev. 57(2):279-88 International Union of Pharmacology. XLVI. G protein-coupled receptor list. http://www.ncbi.nlm.nih.gov/pubmed/15914470
12. Conn PJ, Pin JP (1997) Annu Rev Pharmacol Toxicol. 37():205-37. Pharmacology and functions of metabotropic glutamate receptors. http://www.ncbi.nlm.nih.gov/pubmed/9131252/
13. Ramano et al (1996) J Biol Chem. 8;271(45):28612-6. Metabotropic glutamate receptor 5 is a disulfide-linked dimer. http://www.ncbi.nlm.nih.gov/pubmed/8910492
14. Pin and Acher (2002) The metabotropic glutamate receptors: structure, activation mechanism and pharmacology.Curr Drug Targets CNS Neurol Disord. ;1(3):297-317. http://www.ncbi.nlm.nih.gov/pubmed/12769621
15. Gerber U et al (2007) Metabotropic glutamate receptors: intracellular signaling pathways. Curr Opin Pharmacol. 7(1):56-61. http://www.ncbi.nlm.nih.gov/pubmed/17055336/
16. Ferraguti et al (2008) Metabotropic glutamate 1 receptor: current concepts and perspectives.Pharmacol Rev. 60(4):536-81. http://www.ncbi.nlm.nih.gov/pubmed/19112153/
17. Gladding et al (2009) Metabotropic glutamate receptor-mediated long-term depression: molecular mechanisms. Pharmacol Rev. 61(4):395-412. http://www.ncbi.nlm.nih.gov/pubmed/19926678
18. Mukherjee S, Manahan-Vaughan D (2013). Role of metabotropic glutamate receptors in persistent forms of hippocampal plasticity and learning. Neuropharmacology. 2013 66:65-81. http://www.ncbi.nlm.nih.gov/pubmed/22743159
19. Mannaioni and Conn, (2001) Metabotropic glutamate receptors 1 and 5 differentially regulate CA1 pyramidal cell function. J. Neurosci., 21:5925–5934 http://www.ncbi.nlm.nih.gov/pubmed/1487615
20. Bockaert et al., (2010) GPCR interacting proteins (GIPs) in the nervous system: roles in physiology and pathologies. Ann. Rev. Pharmacol. Toxicol., 50:89–109 http://www.ncbi.nlm.nih.gov/pubmed/20055699
21. Dolen et al (2008) Role for metabotropic glutamate receptor 5 (mGluR5) in the pathogenesis of fragile X syndrome. J Physiol. 15;586(6):1503-8 http://www.ncbi.nlm.nih.gov/pubmed/18202092
22. D'Antoni et al (2014) Dysregulation of group-I metabotropic glutamate (mGlu) receptor mediated signalling in disorders associated with Intellectual Disability and Autism. Neurosci Biobehav Rev. 46 Pt 2:228-41. http://www.ncbi.nlm.nih.gov/pubmed/24548786

 Facebook
Facebook

 LINE
LINE